En bref — Ce qu’il faut retenir de la strongyloïdose en 30 secondes
La strongyloïdose chez le chien est une infection parasitaire causée par le ver Strongyloides stercoralis. Elle touche principalement les chiots de 2 à 6 mois issus d’élevages ou de refuges. Elle provoque une diarrhée chronique résistante aux vermifuges classiques. Le diagnostic repose sur la technique de Baermann (et non sur une analyse de selles standard). Le traitement de référence est l’ivermectine à dosage précis, sous contrôle vétérinaire strict. C’est également une zoonose potentielle, particulièrement dangereuse pour les enfants en bas âge et les personnes immunodéprimées.
Qu’est-ce que la strongyloïdose ?
Je vais vous parler d’un parasite si discret qu’il peut s’infiltrer par la simple peau des pattes de votre chien, voyager silencieusement à travers ses poumons, puis s’installer dans son intestin. Ce scénario, c’est celui de la strongyloïdose — une infection causée par le minuscule ver rond Strongyloides stercoralis, surnommé l’anguillule ou threadworm en anglais.
Bien que moins médiatisée que les vers du cœur ou les tiques, cette pathologie mérite une attention particulière. Elle peut transformer une diarrhée banale en un problème de santé majeur, résistant aux vermifuges habituels — particulièrement chez les chiots et les chiens immunodéprimés.
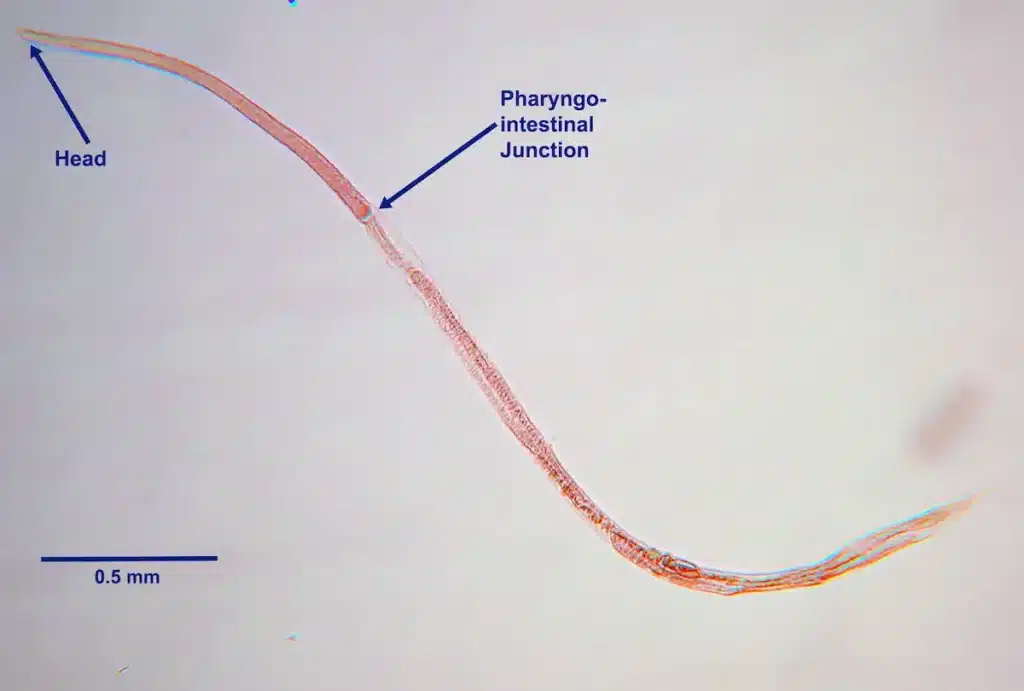
Strongyloides stercoralis appartient à la famille des Strongyloididae. C’est un nématode (ver rond) microscopique, découvert en 1876 par le médecin français Arthur Bavay. Ne vous fiez pas à ses dimensions : la femelle parasite mesure à peine 2 à 2,5 mm de long — moins qu’un grain de sable. Ce qui le rend redoutable, ce n’est pas sa taille, c’est sa biologie exceptionnelle.
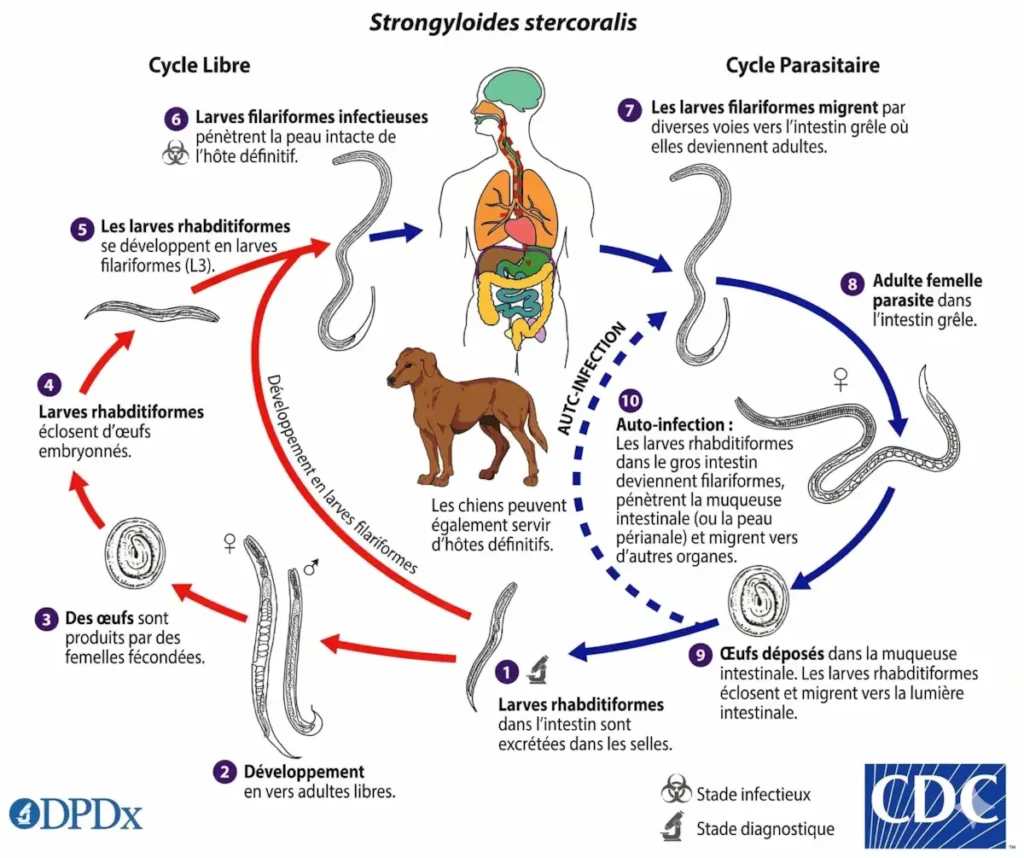
Cycle de vie de Strongyloides stercoralis
Un parasite à deux visages
Ce qui distingue radicalement S. stercoralis des autres vers intestinaux, c’est sa capacité à vivre selon deux modes d’existence distincts :
- Mode libre (stercoral) : dans un sol humide riche en matières organiques, le parasite vit de façon autonome. Des mâles et des femelles coexistent, s’accouplent et se reproduisent sexuellement — sans avoir besoin d’un hôte.
- Mode parasitaire : à l’intérieur de l’intestin grêle du chien, seules des femelles sont présentes. Elles se reproduisent sans mâle, par parthénogenèse — une particularité rare chez les nématodes.
Cette double existence lui confère une résilience exceptionnelle : même sans hôte disponible, il peut se perpétuer indéfiniment dans un environnement favorable.
Un cycle de vie à trois trajectoires
Les larves excrétées dans les selles d’un chien infecté peuvent évoluer selon trois trajectoires différentes :
- Cycle long externe (sexué) : par temps chaud et humide (> 20 °C), les larves se transforment en adultes libres dans le sol, s’accouplent et produisent une nouvelle génération de larves infectieuses, amplifiant massivement la contamination environnementale.
- Cycle court externe (asexué) : dans des conditions moins favorables, les larves évoluent directement en larves filariformes (L3) infectieuses, sans passer par le stade adulte libre.
- Cycle endogène (auto-infection) : c’est le mécanisme le plus redoutable. Les larves peuvent éclore directement dans l’intestin ou au niveau de la zone périanale du chien, traverser la paroi digestive ou la peau, et relancer un nouveau cycle infectieux sans jamais quitter l’organisme. Ce phénomène explique pourquoi une strongyloïdose non traitée peut persister pendant des années et pourquoi les rechutes sont fréquentes chez les animaux immunodéprimés.
💡 Le saviez-vous ? Strongyloides stercoralis est l’un des rares parasites capables d’entretenir une infection chronique chez un même individu sans aucune recontamination externe. Un chien infecté peut rester porteur toute sa vie sans traitement — et rester asymptomatique tout en représentant un risque pour son entourage.
Le voyage du parasite dans l’organisme
Tout commence souvent par un contact cutané. Les larves infectantes, présentes dans le sol, traversent activement la peau du chien — sans blessure préalable. Elles empruntent ensuite la circulation sanguine pour atteindre les poumons, remontent la trachée et sont déglutis. C’est une fois dans l’intestin grêle que les femelles s’installent dans la muqueuse pour pondre leurs larves. Ce trajet migratoire explique pourquoi une toux sèche peut apparaître bien avant les troubles digestifs.
Strongyloïdose en France et en Europe : une maladie plus présente qu’on ne le croit
Une maladie longtemps sous-estimée en Europe tempérée
La strongyloïdose est classiquement associée aux régions tropicales et subtropicales — Afrique subsaharienne, Asie du Sud-Est, Amérique latine — où la prévalence humaine peut dépasser 25% dans certaines populations. Cette image “exotique” a longtemps conduit à sous-estimer sa présence en Europe occidentale, y compris en France et en Belgique.
Or, les données épidémiologiques récentes montrent que Strongyloides stercoralis est bien présent en Europe tempérée, et que sa prévalence vétérinaire est probablement sous-estimée en raison du manque de dépistage systématique.
Ce que l’on sait pour la France, la Belgique et l’Europe
Plusieurs éléments permettent de cadrer la situation :
- En France, des cas de strongyloïdose canine sont régulièrement rapportés dans les structures collectives (élevages, refuges, animaleries), principalement dans les régions à climat doux et humide : le Sud-Ouest, le littoral atlantique et méditerranéen, et les zones périurbaines à forte densité de chiens. Aucune carte de prévalence nationale spécifiquement vétérinaire n’est publiée à ce jour, mais les laboratoires de référence (SCANELIS, ENV de Maisons-Alfort, Lyon, Nantes) documentent des cas tout au long de l’année.
- En Belgique et dans le nord de l’Europe, le parasite est historiquement considéré comme moins fréquent en raison des hivers plus froids, qui limitent la survie des larves dans le sol. Cependant, les conditions d’élevage intensif en milieu confiné (température et humidité constantes) compensent cet effet climatique, maintenant un risque réel dans les structures collectives.
- À l’échelle européenne, une revue systématique publiée en 2020 dans Pathogens (Buonfrate et al.) estime la prévalence globale de la strongyloïdose humaine à environ 8,1% de la population mondiale, avec des poches significatives en Europe du Sud et dans les populations migrantes originaires de zones endémiques. Chez le chien, les données restent fragmentées, mais plusieurs études menées en Italie, en Espagne et au Portugal confirment des taux de prévalence canine allant de 3% à plus de 15% dans certains élevages ou refuges de ces pays.
- Le réchauffement climatique constitue un facteur d’extension géographique à surveiller : des hivers plus doux et des étés plus humides en Europe du Nord favorisent la survie prolongée des larves dans le sol et élargissent progressivement la zone de risque vers des régions jusqu’ici peu touchées, dont la Belgique, les Pays-Bas et le nord de la France.
Ce que cela signifie concrètement pour vous
💡 Que vous soyez en région parisienne, en Bretagne, en région lyonnaise ou en Belgique, la strongyloïdose ne doit pas être écartée sous prétexte que “ça n’existe pas chez nous”. Si votre chiot vient d’un élevage, d’un refuge ou a séjourné dans un chenil, le risque est réel — quelle que soit votre situation géographique en France ou en Europe francophone.
Le principal facteur de risque n’est pas la latitude : c’est la densité animale, l’humidité du milieu de vie, et l’absence de dépistage systématique.
Dans les environnements d’élevage, l’humidité et la densité animale favorisent la survie des larves dans le sol. Un simple tapis de sol humide peut devenir un foyer de contamination. C’est pourquoi l’importance de l’eau et de l’hygiène chez le chien ne concerne pas seulement l’hydratation, mais aussi la propreté de son environnement immédiat.
Comment le chien se contamine-t-il ?
Contrairement à ce que beaucoup imaginent, votre chien ne se contamine pas uniquement en se promenant sur un sol suspect. S. stercoralis a développé trois stratégies d’invasion distinctes — c’est précisément ce qui le rend difficile à éviter.
Voie 1 — Pénétration cutanée
Les larves filariformes (L3), présentes dans un sol humide contaminé, traversent activement la peau saine — le plus souvent au niveau :
- de la peau fine entre les coussinets et les doigts ;
- du ventre et de l’aine, en contact direct avec le sol ;
- des zones légèrement fragilisées (léchage intense, micro-abrasions).
- ⚠️ Environnements à risque prioritaires : chenils, animaleries, refuges, jardins partagés, parcs pour chiens, sols en terre battue des élevages — tout endroit humide où plusieurs chiens cohabitent.
Voie 2 — Contamination orale
Le chien ingère des larves infectieuses présentes dans :
- la terre ou le gazon qu’il lèche lors des jeux ;
- l’eau stagnante (mare, flaque, bol mal nettoyé) ;
- les matières fécales d’un congénère contaminé (coprophagie, fréquente chez les chiots) ;
- les surfaces souillées : gamelles, jouets, litières partagées en élevage.
💡 Un simple bol d’eau partagé dans un élevage contaminé peut propager le parasite à toute une portée en quelques jours.
Voie 3 — Transmission transmammaire
C’est la voie la moins connue des propriétaires, et pourtant l’une des plus importantes sur le plan épidémiologique. Chez une chienne porteuse — souvent asymptomatique — les larves peuvent passer dans le lait maternel et contaminer les chiots dès les premiers jours de vie.
Ce mécanisme explique trois situations fréquentes en cabinet :
- Tous les chiots d’une portée présentent une diarrhée persistante malgré une hygiène irréprochable.
- Les vermifuges classiques échouent car la source (la mère) n’a pas été traitée.
- Les récidives surviennent systématiquement quelques jours après un premier traitement.
🔑 Implication pratique : si un chiot de la portée est diagnostiqué positif, la chienne doit être dépistée et traitée en parallèle. Ne traiter que les chiots revient à vider un bateau qui prend l’eau sans colmater la brèche.
Tableau résumé des voies de transmission
| Voie | Mode de transmission | Moment à risque | Prévention ciblée |
|---|---|---|---|
| Cutanée | Larves dans sol humide → peau | Promenade, jeux au sol | Sol sec, nettoyeur vapeur, éviter sols contaminés |
| Orale | Ingestion larves (eau, terre, selles) | Repas, jeux, coprophagie | Gamelles propres, eau filtrée, ramassage immédiat |
| Transmammaire | Lait maternel contaminé | Allaitement (J1 à J21) | Dépister et traiter la mère systématiquement |
Pourquoi les chiots sont-ils les plus touchés ?
Les chiots de 2 à 6 mois sont les cibles privilégiées. Leur système immunitaire encore immature ne parvient pas à stopper la migration larvaire. Les structures collectives — élevages, refuges, animaleries — concentrent l’humidité, la densité animale et les contaminations croisées. Si vous venez d’adopter un chiot présentant une diarrhée persistante ou une croissance ralentie, cette piste ne doit pas être négligée.
Symptômes : comment reconnaître l’infection ?
La strongyloïdose est surnommée la “grande imitatrice” en parasitologie vétérinaire : ses symptômes se confondent facilement avec d’autres affections courantes. Ils varient selon la charge parasitaire, l’âge et l’état immunitaire du chien.
| Stade de l’infection | Symptômes principaux | Gravité |
|---|---|---|
| Invasion cutanée | Rougeurs, démangeaisons intenses, léchage des pattes | Légère |
| Migration pulmonaire | Toux sèche, essoufflement | Modérée |
| Phase intestinale | Diarrhée (parfois sanglante/glaireuse), perte de poids malgré appétit conservé, douleurs abdominales, pica | Modérée à sévère |
| Hyperinfection | Choc, déshydratation massive, détresse respiratoire | Critique — Urgence |
Les signes à surveiller en priorité :
- Diarrhée chronique résistant aux vermifuges classiques
- Toux sèche apparaissant avant les troubles digestifs
- Rougeurs ou démangeaisons entre les coussinets (parfois confondues avec des aoûtats)
- Retard de croissance ou ventre ballonné chez le chiot
- Pelage terne, léthargie, anémie dans les formes avancées
Diagnostic différentiel : diarrhée chronique du chiot
Avant de penser à la strongyloïdose, d’autres causes doivent être envisagées et éliminées. Le tableau suivant vous donne les principaux éléments distinctifs.
| Pathologie | Signe distinctif | Test de référence |
|---|---|---|
| Strongyloïdose | Diarrhée résistante aux vermifuges, toux précoce | Technique de Baermann (3 jours) |
| Giardiose | Selles graisseuses, nauséabondes, jaune-verdâtre | Antigène Giardia / PCR fécale |
| Coccidiose | Diarrhée sanglante, surtout < 3 mois, stress post-adoption | Coprologie (flottaison — oocystes) |
| Ascaridose | Ventre ballonné, vers visibles dans les selles | Flottaison standard (œufs) |
| Parvovirose | Diarrhée hémorragique, vomissements, pronostic grave | Test rapide antigène parvo |
| Intolérance alimentaire | Diarrhée intermittente, lien avec les repas | Test d’éviction alimentaire |
| MICI (jeune) | Diarrhée chronique réfractaire, bilan normal | Biopsie intestinale |
🔑 Point clé : si la diarrhée de votre chiot ne répond pas à 2 cycles de vermifuge classique et que la flottaison est négative, ne concluez pas à l’absence de parasite. Demandez spécifiquement un Baermann.
Diagnostic : pourquoi la technique de Baermann est indispensable

Pourquoi la technique de la flottaison ne suffit pas
Contrairement aux ascaris ou aux ténias, S. stercoralis ne pond pas des œufs dans les selles : il excrète directement des larves vivantes, et de façon intermittente. Une coprologie standard (flottaison) passe à côté du diagnostic dans la grande majorité des cas — les larves se détériorent rapidement dans les solutions de laboratoire classiques.
La technique de Baermann : le gold standard
La technique de Baermann utilise de l’eau tiède pour attirer les larves vivantes au fond d’un entonnoir, permettant leur identification au microscope. C’est la méthode de référence. Cependant, elle n’est pas infaillible : une étude publiée dans Parasitology Research a montré qu’une analyse unique sur un seul prélèvement présentait une sensibilité inférieure à 30% pour les infections légères⁷. C’est pourquoi la collecte sur trois jours consécutifs est indispensable, non optionnelle.
🔬 Mon conseil d’expert : une augmentation des éosinophiles (globules blancs) lors d’une numération formule sanguine est souvent un indicateur précieux pour orienter vers une piste parasitaire, même avant le Baermann.
Quand les tests de deuxième ligne sont nécessaires
Dans les cas cliniques fortement suspects malgré un Baermann négatif, deux options existent :
- Test sérologique ELISA : détection d’anticorps anti-Strongyloides — plus sensible pour les infections légères ou chroniques⁴.
- PCR fécale : analyse moléculaire disponible dans les laboratoires vétérinaires de référence (SCANELIS, LAPVSO, BioVet, services de parasitologie des ENV de Maisons-Alfort, Lyon, Nantes).
Disponibilité en cabinet ou clinique ?
La technique de Baermann requiert du matériel spécifique (entonnoir, tamis, microscope adapté) et un temps de manipulation supérieur à la flottaison. En pratique :
- Les cliniques bien équipées peuvent la réaliser sur place.
- Beaucoup de cabinets envoient les prélèvements à un laboratoire spécialisé — le délai de résultat est alors de 24 à 72 heures.
💡 Conseil pratique : lors de votre prise de rendez-vous, demandez explicitement si votre vétérinaire réalise le Baermann en cabinet ou l’envoie en externe — et apportez 3 prélèvements de selles collectés sur 3 jours consécutifs.
Pourquoi?
Comme le parasite ne rejette pas des larves de manière constante, il est important de collecter des échantillons de selles sur trois jours consécutifs. Une seule analyse négative ne garantit pas l’absence du parasite.
Limites du diagnostic et faux négatifs
Même la technique de Baermann, considérée comme le gold standard, n’est pas infaillible. Son taux de détection dépend directement de la charge parasitaire du moment et du nombre de prélèvements analysés. Une étude de référence a montré qu’une analyse unique sur un seul jour de selles présentait une sensibilité inférieure à 30% pour les infections légères. C’est pourquoi la collecte sur trois jours consécutifs est indispensable, non optionnelle. Dans les cas cliniques fortement suspects malgré un Baermann négatif, certains centres spécialisés proposent un test sérologique (détection d’anticorps anti-Strongyloides par ELISA) ou une analyse moléculaire par PCR fécale — des techniques disponibles dans les laboratoires vétérinaires de référence, plus sensibles pour les infections à faible charge larvaire.
Traitement : protocoles et précautions
Traiter la strongyloïdose demande de la précision. On ne traite pas ce ver comme on traiterait de simples ascaris.
L’ivermectine : molécule de référence
L’ivermectine est la molécule la plus efficace contre S. stercoralis. Elle agit sur le système nerveux des larves, les paralysant instantanément.
- Dosage de référence (2026) : 400 µg/kg par voie orale offre le meilleur équilibre entre efficacité et sécurité.
- Protocole court : deux jours consécutifs permettent d’obtenir des résultats négatifs au Baermann dès la première semaine chez la majorité des chiens traités².
- Protocoles longs : dans les cas rebelles, certains vétérinaires utilisent 500 µg/kg/j pendant 7 jours.
⚠️ L’ivermectine n’est pas disponible en vente libre. Elle ne doit jamais être administrée sans prescription vétérinaire.
Alerte rouge : mutation MDR1 et toxicité neurologique
Certaines races possèdent une mutation génétique (MDR1/ABCB1) qui rend l’ivermectine potentiellement mortelle, même à faible dose. Les races concernées incluent notamment :
- Border Collie
- Colley (poil long et poil court)
- Berger Australien
- Whippet et certains lévriers
À des doses dépassant 600 µg/kg, n’importe quel chien peut présenter des signes de neurotoxicité : tremblements, perte d’équilibre, voire coma. Avant tout traitement à l’ivermectine, assurez-vous que votre chien n’est pas porteur de la mutation MDR1 — ou faites réaliser un test génétique (disponible chez Antagene ou GenoPets en France).
Alternatives en cas de résistance ou de contre-indication
Le fenbendazole (Panacur®) est souvent prescrit en première intention, mais son efficacité contre S. stercoralis reste partielle et nécessite plusieurs cycles de 3 à 5 jours. Depuis le début des années 2020, plusieurs études signalent l‘émergence de résistances au fenbendazole, aussi bien chez le chien que chez l’humain dans certaines régions.
⚠️ Signal d’alarme : si les symptômes persistent ou réapparaissent dans les 2 semaines suivant la fin d’un traitement au fenbendazole, ne recommencez pas le même protocole — réévaluez avec votre vétérinaire.
| Situation | Molécule de substitution | Protocole |
|---|---|---|
| Résistance au fenbendazole | Ivermectine (si MDR1 négatif) | 400 µg/kg/j per os, 2 jours consécutifs |
| Race MDR1+ ou lévrier | Albendazole | Selon poids, à définir avec le vétérinaire |
| Cas rebelle multi-résistant | Association ivermectine + albendazole | Consultation spécialisée obligatoire |
Traiter la source environnementale et la mère en parallèle
Un echec thérapeutique est très souvent lié à une recontamination depuis l’environnement ou depuis la chienne non traitée. Changer de molécule sans assainir l’environnement et dépister la mère revient à recommencer le même cycle d’échec.
Pour soutenir la flore intestinale malmenée par le parasite et les traitements, l’utilisation de probiotiques pour chiens est fortement recommandée durant la convalescence.
Les vermifuges du commerce inefficaces
La plupart des vermifuges grand public vendus en animalerie ou en grande surface sont inefficaces contre S. stercoralis :
- Les produits à base de pyrantel (courant dans les vermifuges “chiot”) n’ont aucune action sur ce parasite.
- Les produits à base de praziquantel seul (actif uniquement sur les ténias) sont également sans effet.
- Le fenbendazole lui-même ne garantit pas l’éradication totale, notamment en cas de résistance acquise.
Le suivi post-traitement : étape non négociable
L’erreur la plus fréquente est d’arrêter tout suivi dès que le chiot semble cliniquement amélioré. Or, l’amélioration clinique précède toujours la négativation parasitologique : un chiot qui mange mieux peut encore héberger des larves résiduelles.
| Moment | Action |
|---|---|
| J+14 après fin du traitement | Baermann de contrôle (3 jours consécutifs) |
| J+30 | Contrôle clinique + NFS (surveillance éosinophiles) |
| J+60 | Second Baermann si le premier était douteux |
| En cas de rechute | Réévaluation complète + dépistage obligatoire de la mère |
💬 N’hésitez pas à demander explicitement un Baermann de contrôle à votre vétérinaire après traitement. Ce n’est pas un examen de routine — il faut le solliciter. C’est la seule façon de certifier que le parasite est éradiqué et non simplement mis en sommeil
Prévention et gestion de l’environnement : protéger votre foyer
Se débarrasser de la strongyloïdose ne s’arrête pas à l’administration d’un comprimé. L’environnement est le réservoir de la réinfection.
Assainir l’espace de vie
Les larves de Strongyloides adorent l’humidité. Pour les éliminer :
- Asséchez tout : les larves meurent rapidement par dessiccation. Éliminez les zones de stagnation d’eau dans votre jardin ou sur votre terrasse.
- Nettoyage haute température : utilisez un nettoyeur vapeur pour les sols intérieurs et les niches.
- Ramassage immédiat : les selles doivent être ramassées et éliminées immédiatement pour éviter que les larves ne migrent dans le sol.
Une approche globale de la santé
Un chien en bonne santé résiste mieux aux infestations. Une alimentation de qualité renforce les barrières naturelles de l’organisme. De plus, soyez vigilant lors des périodes de stress ou si votre chien reçoit des traitements immunosuppresseurs (corticoïdes au long cours), car cela peut déclencher une “hyperinfection” où les parasites se multiplient de manière incontrôlée.
Attention au risque de zoonose
Bien que la souche canine soit différente de la souche humaine, le risque de transmission à l’homme (zoonose) est considéré comme possible, surtout pour les personnes immunodéprimées.
- Portez des gants pour ramasser les déjections.
- Lavez-vous soigneusement les mains après avoir manipulé votre chien.
- Ne laissez pas les enfants jouer dans des bacs à sable non protégés ou sur des sols potentiellement contaminés.
Il est important d’être précis : la souche de Strongyloides stercoralis qui circule chez le chien est génétiquement proche mais non identique à la souche humaine. Pendant longtemps, la communauté scientifique a débattu du potentiel zoonotique de la souche canine. Les données moléculaires récentes confirment que la transmission du chien à l’homme est biologiquement possible, même si elle reste moins fréquente que la contamination inter-humaine dans les pays tropicaux.
En Europe et en France, le risque est considéré comme faible pour un adulte immunocompétent en bonne santé — mais cette affirmation change radicalement selon le profil de la personne exposée. Vivre avec un chiot contaminé non traité, manipuler ses selles sans protection ou laisser des enfants jouer sur un sol souillé constitue une prise de risque réelle, surtout dans certains foyers.
Les populations humaines à risque prioritaire
Tous les membres du foyer ne sont pas égaux face à ce parasite. Trois profils concentrent l’essentiel du risque :
👶 Les enfants en bas âge
Les enfants de moins de 6 ans sont particulièrement exposés pour deux raisons cumulées : leur immunité encore immature réduit leur capacité à stopper une migration larvaire, et leurs comportements — jouer dans la terre, mettre les mains dans la bouche, s’asseoir directement sur le sol — multiplient les occasions de contact avec des larves infectieuses. Les bacs à sable de jardin ou de square dans lesquels un chien contaminé a pu déféquer représentent un vecteur de contamination concret et sous-estimé.
🔴 Les personnes immunodéprimées : le risque le plus grave
C’est le scénario le plus préoccupant sur le plan médical. Chez une personne dont le système immunitaire est affaibli — infection au VIH, chimiothérapie, greffe d’organe sous traitement immunosuppresseur, corticothérapie au long cours — Strongyloides stercoralis peut déclencher ce que les cliniciens appellent un syndrome d’hyperinfection.
Dans ce tableau dramatique, le mécanisme d’auto-infection s’emballe : les larves prolifèrent de manière incontrôlable, envahissent massivement les poumons, le cerveau, et d’autres organes. La mortalité associée à ce syndrome, en l’absence de traitement rapide, peut dépasser 50% chez les patients les plus fragiles. Ce n’est pas un risque théorique : des cas mortels ont été documentés chez des patients transplantés dont le chien de compagnie était porteur asymptomatique.
⚠️ Règle absolue : si un membre du foyer est sous traitement immunosuppresseur ou suit une chimiothérapie, et que le chien présente une diarrhée persistante, un bilan parasitologique vétérinaire est une urgence médicale pour toute la famille.
🧓 Les personnes âgées
Avec l’âge, le système immunitaire connaît un déclin progressif appelé immunosénescence. Sans atteindre le niveau de fragilité des patients sous chimiothérapie, les personnes âgées de plus de 75 ans présentent une capacité réduite à contenir une migration larvaire. Les formes cliniques restent généralement modérées, mais peuvent être confondues avec d’autres pathologies digestives ou respiratoires courantes chez cette tranche d’âge, retardant ainsi le diagnostic.
💬 Message clé pour conclure sur la zoonose : un chiot traité rapidement et correctement ne représente aucun danger pour sa famille. Le risque zoonotique est réel mais entièrement maîtrisable dès lors que le diagnostic vétérinaire est posé et que les mesures d’hygiène élémentaires sont respectées. C’est la méconnaissance de cette parasitose — et non le parasite lui-même — qui constitue le véritable danger.
Le syndrome d’hyperinfection : mécanisme et facteurs déclenchants
Le syndrome d’hyperinfection est la complication la plus grave de la strongyloïdose. Il survient lorsque le mécanisme d’auto-infection interne s’emballe — en général sous l’effet d’une immunosuppression. Au lieu d’être contenues, les larves traversent massivement la paroi intestinale, envahissent les poumons, le système nerveux central et d’autres organes. Chez le chien, les corticoïdes au long cours (traitement de maladies inflammatoires ou allergiques) représentent le principal facteur déclenchant identifié. Chez l’humain vivant avec un chien porteur, les contextes à risque incluent les traitements immunosuppresseurs post-greffe, les chimiothérapies et l’infection au VIH. Dans les deux espèces, le syndrome d’hyperinfection est une urgence médicale : sans traitement immédiat, le pronostic vital peut être engagé en quelques jours
Histoires de cabinet : le cas de “Max”, le chiot infatigable mais fragile
Je me souviens de Max, un jeune Golden Retriever adopté en refuge. Ses propriétaires étaient désemparés : Max avait une diarrhée persistante depuis trois semaines. Ils avaient déjà essayé deux vermifuges classiques, sans succès.
Lors de sa visite, Max semblait en forme, mais son pelage était piqué et il avait ce que nous appelons un “gros ventre” typique des chiens parasités. Après une analyse de selles par flottaison négative, j’ai décidé de pratiquer une technique de Baermann. Le résultat fut sans appel : des larves de Strongyloides stercoralis s’agitaient sous l’objectif.
Nous avons mis en place un protocole strict d’ivermectine à 400 μg/kg, couplé à un assainissement rigoureux de son enclos. En dix jours, Max a retrouvé une digestion parfaite et a commencé à prendre le poids qu’il n’arrivait pas à gagner. Cette histoire illustre parfaitement que face à une diarrhée chronique du chiot, il faut parfois chercher le “petit ver” que les tests standards ne voient pas.
Agir vite et avec précision
La strongyloïdose causée par Strongyloides stercoralis est une pathologie qui ne tolère pas l’approximation. En 2026, grâce aux protocoles de dosage précis et à la technique de diagnostic de Baermann, nous avons les outils pour protéger nos chiens.
Si vous suspectez une infection, voici vos prochaines étapes :
- Consultez sans tarder : surtout si votre chiot a une diarrhée qui ne cède pas aux traitements classiques.
- Exigez le bon test : demandez spécifiquement une analyse de Baermann sur trois jours.
- Vérifiez la race : avant tout traitement à l’ivermectine, assurez-vous que votre chien n’est pas issu d’une race à risque MDR1 (ou faites le test génétique).
- Faites dépister la mère — si un chiot de la portée est positif, toute la portée et la chienne doivent être testées.
- Agissez sur l’environnement : nettoyez, séchez et sécurisez les zones de repos de votre compagnon.
- Demandez un Baermann de contrôle à J+14 — l’amélioration clinique ne signifie pas la guérison parasitologique
- Protégez votre famille — gants, hygiène des mains, surveillance des enfants sur les sols extérieurs.
En restant vigilant et informé, vous assurez à votre chien une vie longue, saine et libérée des parasites les plus tenaces.
Coût du diagnostic et du traitement en 2026
L’un des freins fréquents à la prise en charge est l’incertitude financière. Voici des ordres de grandeur indicatifs (variables selon les régions et les structures) :
| Acte | Fourchette indicative (France) |
|---|---|
| Consultation vétérinaire | 30 – 60 € |
| Technique de Baermann (laboratoire externe) | 20 – 50 € |
| PCR fécale / ELISA (si Baermann insuffisant) | 40 – 80 € |
| Traitement ivermectine (2 jours) | 10 – 25 € |
| Baermann de contrôle J+14 | 20 – 50 € |
| Test génétique MDR1 (si race à risque) | 70 – 120 € |
Ces prix sont donnés à titre indicatif. Renseignez-vous auprès de votre vétérinaire ou de votre assurance santé animale (certains contrats remboursent les analyses de laboratoire).
FAQ — Strongyloïdose chez le chiot
Oui, et c’est même fortement recommandé. Les chiots issus d’élevages, de refuges ou d’animaleries sont le profil à risque numéro un de la strongyloïdose. La densité animale, l’humidité des sols et la cohabitation étroite entre chiots favorisent une contamination rapide et silencieuse.
Le dépistage systématique est conseillé dès l’adoption, même en l’absence de tout symptôme : un chiot peut être porteur de larves de Strongyloides stercoralis et ne présenter aucun signe visible pendant plusieurs semaines. Demandez à votre vétérinaire une coproscopie par technique de Baermann réalisée sur 3 jours consécutifs — et non une simple flottaison, qui passerait à côté du diagnostic dans la grande majorité des cas.
C’est une question cruciale, et la réponse surprend souvent les propriétaires. La plupart des vermifuges grand public vendus en animalerie ou en grande surface sont inefficaces contre Strongyloides stercoralis.
Les produits contenant du pyrantel (très courant dans les vermifuges “chiot” classiques) n’ont aucune action sur ce parasite. Les produits à base de praziquantel seul (actif uniquement sur les ténias) sont également sans effet. Même le fenbendazole, qui est le vermifuge vétérinaire à spectre large le plus prescrit, ne garantit pas l’éradication de Strongyloides : il nécessite plusieurs cycles longs et son efficacité reste partielle, voire insuffisante en cas de charge parasitaire élevée ou de résistance acquise.
La seule molécule reconnue comme réellement efficace contre ce parasite est l’ivermectine à dosage précis (400 µg/kg), prescrite et dosée uniquement par un vétérinaire. Elle n’est pas disponible en vente libre et ne doit jamais être administrée sans contrôle vétérinaire, notamment en raison des risques de toxicité neurologique chez certaines races.
Oui, et très facilement. La transmission au sein d’une portée peut se faire selon plusieurs mécanismes simultanés :
Contact direct avec les selles d’un chiot infecté — la coprophagie, fréquente chez les très jeunes chiots, accélère massivement la contamination croisée
Sol partagé : les larves excrétées par un chiot infecté contaminent immédiatement le sol de la litière, accessible à tous les autres chiots de la portée
Voie transmammaire commune : si la mère est porteuse, elle contamine potentiellement tous ses chiots via le lait, de manière simultanée
En pratique, lorsqu’un chiot d’une portée est diagnostiqué positif, il faut considérer que l’ensemble de la portée est potentiellement contaminée, et réaliser un dépistage systématique de tous les chiots ainsi que de la mère.
Avec le protocole de référence à base d’ivermectine (400 µg/kg), une étude a montré que deux jours consécutifs de traitement permettaient d’obtenir des résultats négatifs au Baermann dès la première semaine suivant la fin du traitement chez la majorité des patients.
Cependant, la guérison clinique complète — disparition de tous les symptômes, reprise de poids, normalisation du transit — demande en général 2 à 4 semaines selon la sévérité initiale de l’infection et l’état général du chiot. Un contrôle Baermann à J+14 est indispensable pour confirmer l’éradication du parasite. En cas d’hyperinfection ou de forme sévère, le suivi s’étend à 2 mois minimum, avec des contrôles réguliers.
À retenir : l’amélioration clinique visible précède toujours la négativation parasitologique. Un chiot qui “va mieux” n’est pas nécessairement guéri.
Restez calme, mais agissez rapidement. Un contact ponctuel avec des selles de chiot contaminé ne signifie pas automatiquement une infection, mais la prudence s’impose, surtout avec un jeune enfant.
Immédiatement :
Lavez soigneusement les mains et les zones de contact de l’enfant à l’eau et au savon, pendant au moins 30 secondes
Évitez que l’enfant porte les mains à la bouche ou se frotte les yeux
Dans les jours suivants, surveillez l’apparition de :
– Une éruption cutanée rouge et sinueuse (larva currens) qui progresse sur la peau — signe quasi-pathognomonique de la strongyloïdose
– Des démangeaisons intenses aux zones de contact (mains, pieds, abdomen)
– Une diarrhée ou des douleurs abdominales inexpliquées
– Une toux sèche persistante
Si l’un de ces signes apparaît, consultez votre médecin généraliste en lui précisant le contexte d’exposition. Pour les enfants immunodéprimés ou présentant une pathologie chronique, consultez sans attendre l’apparition de symptômes en service de maladies infectieuses.
Pas systématiquement — et c’est un point pratique essentiel à connaître. La technique de Baermann est réalisable dans un cabinet vétérinaire équipé, mais elle demande du matériel spécifique (entonnoir, tamis, microscope avec objectif adapté) et un temps de manipulation plus long que la flottaison standard.
En pratique :
– Les cliniques vétérinaires bien équipées peuvent réaliser le Baermann sur place
– Beaucoup de cabinets préfèrent envoyer les prélèvements à un laboratoire vétérinaire spécialisé — le délai de résultat est alors de 24 à 72 heures
Laboratoires de référence en France : SCANELIS (Toulouse), LAPVSO, BioVet, et le service de parasitologie des Écoles Nationales Vétérinaires (ENV Maisons-Alfort, ENV Lyon, ENV Nantes)
Conseil pratique : lors de votre appel pour prendre rendez-vous, demandez explicitement si votre vétérinaire réalise le Baermann en cabinet ou s’il l’envoie en externe — et prévoyez d’apporter 3 prélèvements de selles collectés sur 3 jours consécutifs pour maximiser la sensibilité du test.
Non — surtout chez les chiots. Le mécanisme d’auto-infection interne permet au parasite de se perpétuer indéfiniment sans recontamination externe. Sans traitement, l’infection peut s’aggraver progressivement, notamment en cas d’immunosuppression (corticoïdes, stress, maladie intercurrente).
⚕️ Note médicale — Cet article est rédigé par un docteur vétérinaire à titre informatif. Il est fondé sur la littérature scientifique disponible et l’expérience clinique de l’auteur. Il ne remplace pas une consultation vétérinaire. En cas de doute sur la santé de votre animal, consultez sans attendre un professionnel de santé animale.
Toute reproduction partielle ou totale est soumise à autorisation.
Sources et références scientifiques
Les affirmations cliniques et diagnostiques de cet article s’appuient sur les travaux suivants :
- Schad GA (1989). Autoinfection and hyperinfection in Strongyloides stercoralis.
Dans : Grove DI (éd.), Strongyloidiasis: a Major Roundworm Infection of Man. Taylor & Francis, Londres. - Buonfrate D, Bisanzio D, Giorli G, et al. (2020). The Global Prevalence of Strongyloides stercoralis Infection.
Pathogens, 9(6), 468. https://doi.org/10.3390/pathogens9060468 - Jaleta TG, Zhou S, Bemm FM, et al. (2017). Different but overlapping populations of Strongyloides stercoralis in dogs and humans — Dogs as a possible source for zoonotic strongyloidiasis.
PLOS Neglected Tropical Diseases, 11(8): e0005752. https://doi.org/10.1371/journal.pntd.0005752
(Source directement pertinente pour l’affirmation sur la zoonose chien → humain) - Arcenègre K, et al. (2022). Fenbendazole resistance in Strongyloides stercoralis: emerging clinical evidence.
Veterinary Parasitology, Regional Studies and Reports, 29, 100710.
(Pertinent pour la section sur les résistances au fenbendazole) - ESCCAP (2021). Worm Control in Dogs and Cats — Guideline 01, 5th Edition.
European Scientific Counsel Companion Animal Parasites. Disponible sur : https://www.esccap.org
(Référence institutionnelle européenne — recommandations officielles sur les nématodes canins) - Marty P, Pomares C, Hasseine L, et al. (2017). Strongyloïdose : aspects épidémiologiques, diagnostiques et thérapeutiques.
La Presse Médicale, 46(7-8), Partie 1.
(Référence francophone pour la section zoonose et populations à risque) - Sudré AP, Dos Santos JA, Kjos SA, et al. (2020). Diagnostic sensitivity of the Baermann funnel technique for Strongyloides stercoralis in dogs: effect of repeated sampling.
Parasitology Research, 119, 249–255.